Utmaning:
Optimera volumetrisk behandling för ARDS-patienter
Behandlingen som väljs för en kritiskt sjuk patient kan vara livsavgörande. Med ARDS blir detta ännu viktigare eftersom den skadade lungan har en ökad lungpermeabilitet vilket leder till lungödem. Behovet av att på ett tidigt stadium få en tydlig bild av patientens hemodynamiska status för att kunna använda lämplig behandling är avgörande. Behandlingshastigheten påverkar utfallet.
Kan vi kvantifiera lungödem?
Under de senaste tjugo åren har transpulmonell termodilutionsteknik (TPTD) introducerats och utvecklats. [1] Detta möjliggör kvantifiering av lungödem med hjälp av ett index för extravaskulärt lungvatten (ELWI) och ett index för lungkärlspermeabilitet (PVPI). PVPI möjliggör differentialdiagnos av orsaken till lungödem: kardiogen eller permeabilitetsinducerat. ELWI och PVPI kan användas som kriterier som indikerar risken för vätskeadministrering. [2]
Extravaskulärt lungvatten är en ansamling av vätska i lungvävnadens och/eller alveolernas interstitium (mycket små utrymmen). Index för lungkärlspermeabilitet (PVPI) återspeglar indirekt integriteten hos alveolar-kapillärbarriären.
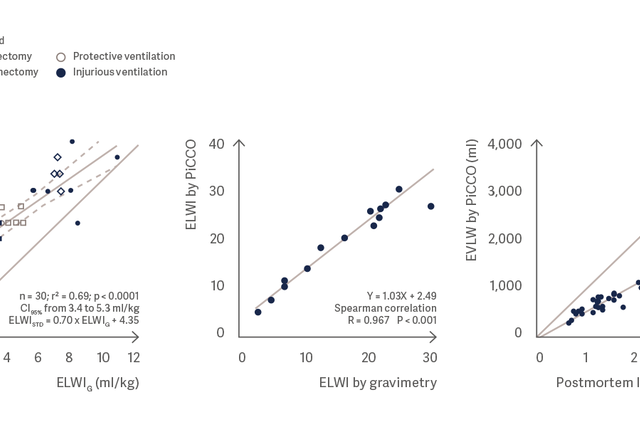
Lungvattenmätningen med PiCCO motsvarar mycket väl den gravimetriska lungvattenmätningen och post mortem-lungvikten. [3], [4], [5]
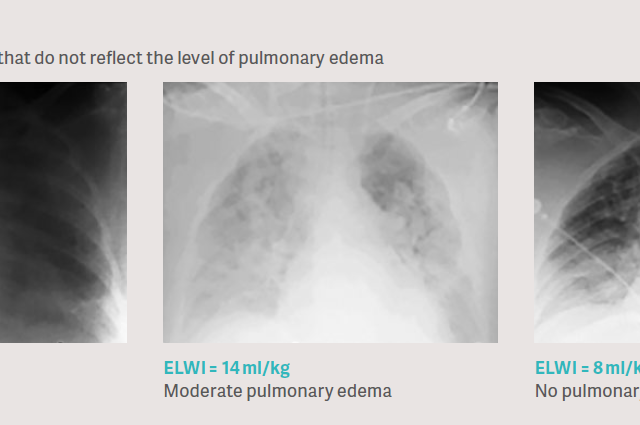
Kliniskt problem: Röntgen av bröstkorgen återger inte lungödemets omfattning på ett tillförlitligt sätt.
Den vanliga kliniska metoden för att bedöma lungödem är att utvärdera en lungröntgen. Detta är mycket svårt eftersom lungröntgen är en densitetsmätning som påverkas av bröstkorgens alla beståndsdelar, såsom ben, muskler, vävnadslager, blod, blodkärl, luft, vävnadsödem, vätskeutgjutning och möjligen även lungödem. I kliniska studier har det därför visats att röntgenundersökning av bröstkorgen för lungödem är mycket inexakt i jämförelse med direkt kvantifiering genom transpulmonell termodilutionsmätning. [6], [7], [8].
Kardiogent eller permeabilitetsinducerat lungödem?
PVPI är en indirekt återspegling av integriteten hos
alveolar-kapillärbarriären. Den beräknas utifrån förhållandet mellan EWLI och pulmonell blodvolym (PBV), förhållandet mellan vätskevolymen som finns utanför kärlen och vätskevolymen som finns kvar inne i kärlen. [9]
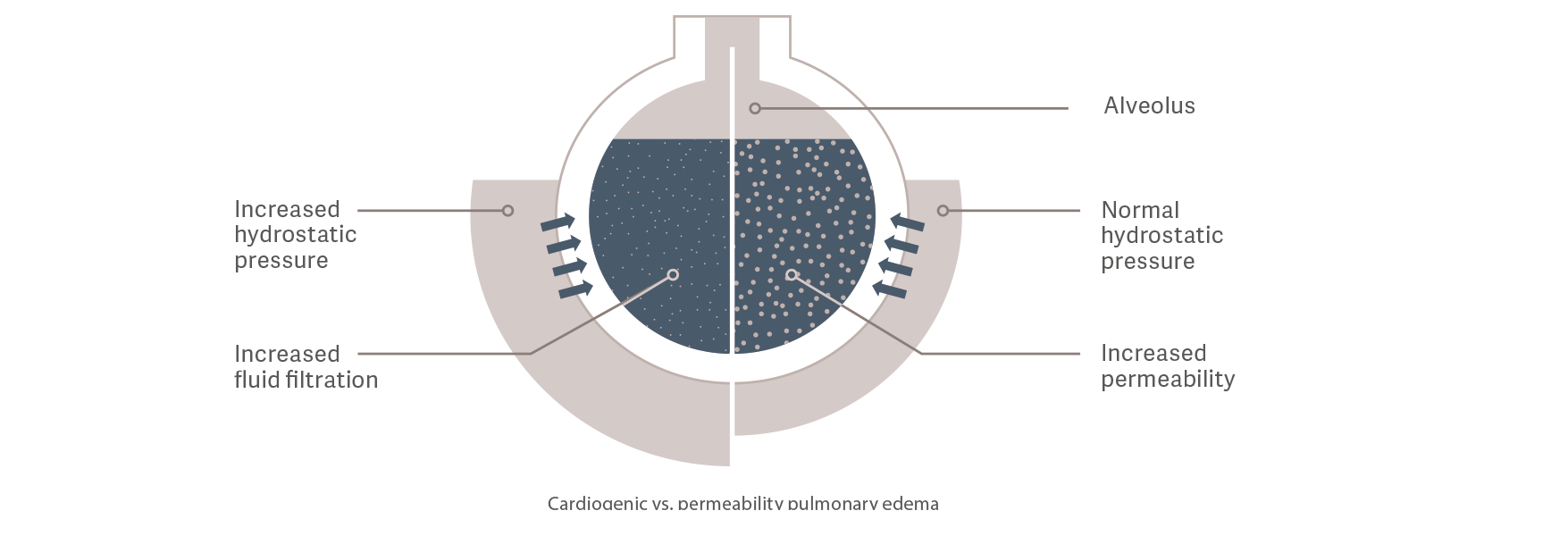
Kardiogent lungödem
Det hydrostatiska trycket ökar på grund av överbelastning av den intravaskulära vätskan.
Detta gör att vätska läcker in i det extravaskulära rummet.
Permeabelt lungödem
Kärlpermeabiliteten ökas på av en inflammatorisk reaktion orsakad av t.ex. sepsis. Detta leder till ökad överföring av vätskor, elektrolyter
och proteiner från det intravaskulära utrymmet till det extravaskulära utrymmet,
även vid normal till låg intravaskulär vätskestatus och hydrostatiskt tryck.
Interaktion mellan ELWI och PVPI har klinisk nytta
Behovet av att identifiera och kvantifiera lungödem vid komplexa syndrom såsom ARDS kan påverka utfallet. Lungödemsansamling försämrar andningsgasutbytet, vilket leder till andningsinsufficiens. Parametrarna ELWI och PVPI kan användas för känslig kvantifiering av lungödem direkt vid patientens säng. De gör det också möjligt att utvärdera allvarlighetsgraden av ARDS. [2]
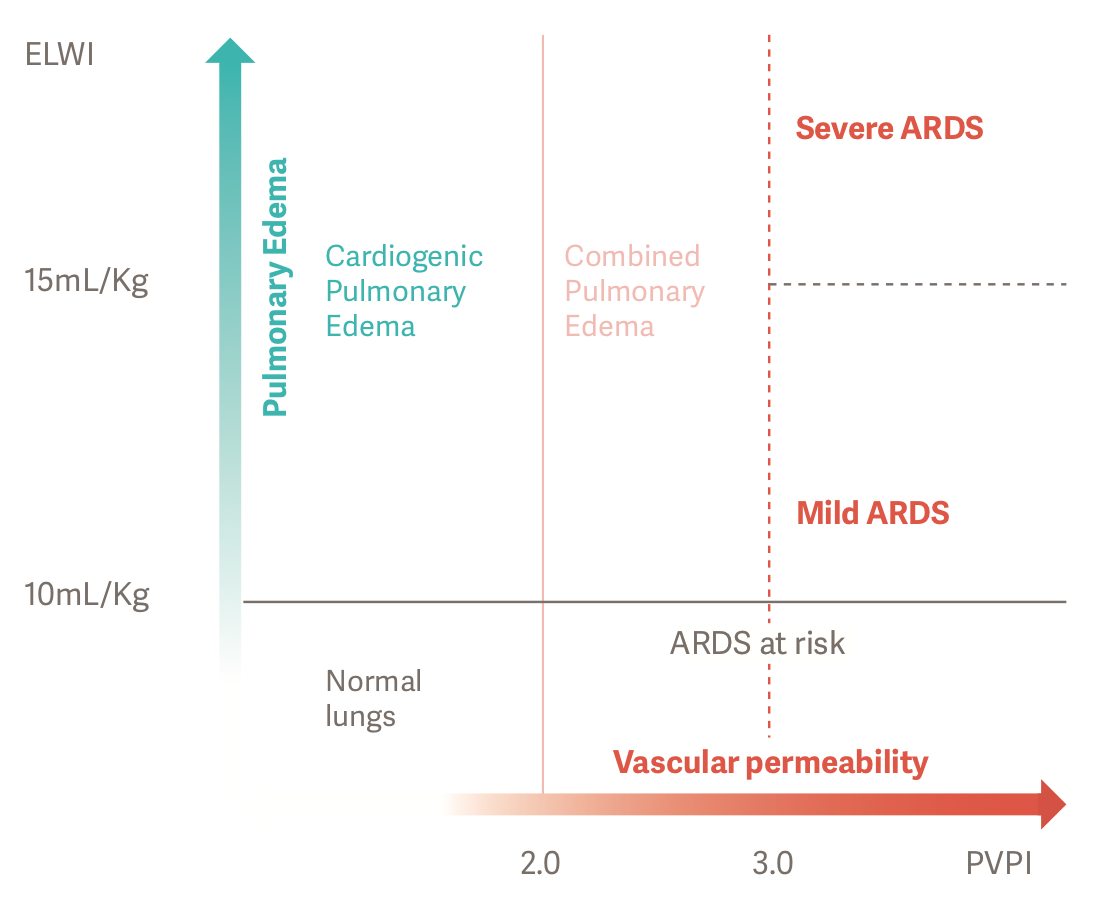
Noggranna och objektiva diagnoser kan ställas på ARDS-patienter med hjälp av ELWI och PVPI. PVPI över 3 med ELWI över 10 ml/kg representerar ökat permeabelt lungödem, eller ARDS.[2],
ARDS-hantering baserad på PiCCO förbättrar utfallet
Inom ramen för ARDS tyder studier på att behandling baserad på protokoll som inkluderar ELWI-mätningar är säker, leder till en lägre kumulativ vätskebalans, sänker dödlighetstalen på IVA samt reducerar behandlingslängden med mekanisk ventilation, IVA-vistelsen och behandlingskostnaderna. [10]
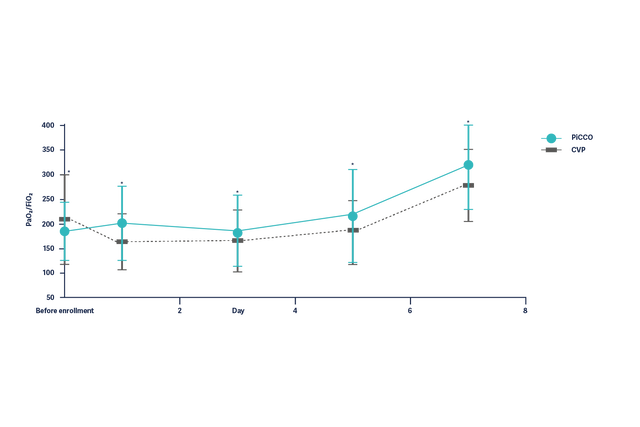
Förbättring i syresättning (PaO2/FiO2) hos ARDS-patienter under 7 dagar är signifikant bättre hos patienter med hemodynamisk behandling baserad på PiCCO-parametrar.