Проблема:
оптимизация волюметрической терапии пациентов с ОРДС
Жизнь пациента в критическом состоянии зависит от правильного выбора следующего этапа терапии. При ОРДС это еще более критично, поскольку пораженное легкое имеет повышенную проницаемость, что приводит к отеку легкого. Необходимость своевременного получения четкого представления о гемодинамическом состоянии пациента очень важно для правильной терапии. Скорость проведения терапии влияет на исход.
Возможно ли количественно измерить отек легких?
В последние два десятка лет появилась и развивается методика транспульмональной термодилюции (TPTD) [1]. Она позволяет количественно оценить отек легких по индексу содержания внесосудистой воды в легких (ELWI) и индексу проницаемости легочных сосудов (PVPI). PVPI позволяет осуществлять дифференциальную диагностику причины отека легких, т. е. дифференцировать кардиогенный отек легких и отек легких, обусловленный проницаемостью. ELWI и PVPI могут использоваться как критерии, указывающие на риск введения жидкости [2].
Внесосудистая вода в легких представляет собой накопление жидкости в интерстициальной ткани легких и (или) альвеолах. Индекс проницаемости легочных сосудов (PVPI) является косвенным показателем целостности альвеолярно-капиллярного барьера.
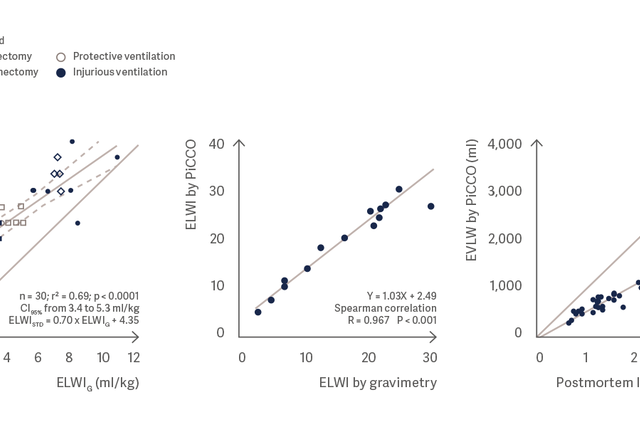
Измерение содержания воды в легких с использованием PiCCO очень хорошо коррелирует с гравиметрическим измерением содержания воды в легких и посмертной массой легких [3], [4], [5].
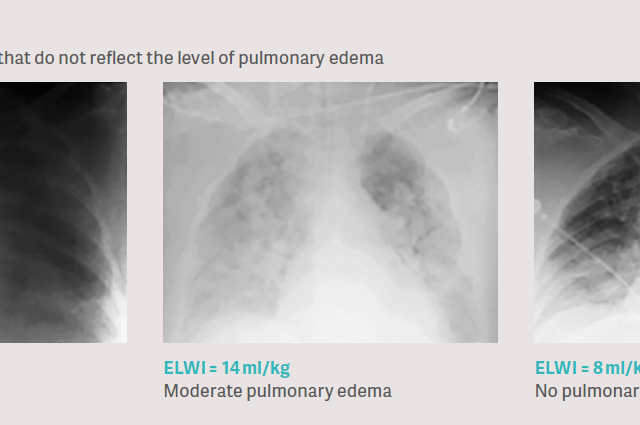
Клиническая проблема: рентгенография органов грудной клетки не показывает степень отека легких с высокой точностью
Обычным клиническим подходом к оценке отека легких является анализ рентгенографии органов грудной клетки. Это создает множество проблем, поскольку рентгенография органов грудной клетки позволяет измерить плотность, а на нее влияют все компоненты грудной клетки, такие как кости, мышцы, слои ткани, кровь, кровеносные сосуды, воздух, тканевой отек, множественный выпот, а также, возможно, отек легких. Таким образом, в клинических исследованиях было показано, что анализ рентгенографии органов грудной клетки при отеке легких очень неточен по сравнению с прямой количественной оценкой методом транспульмональной термодилюции [6], [7], [8].
Кардиогенный отек легких или отек легких, обусловленный проницаемостью?
Индекс проницаемости легочных сосудов (PVPI) представляет собой косвенный показатель целостности альвеолярно-капиллярного
барьера. Он рассчитывается по соотношению EWLI и легочного объема крови (PBV), которое представляет собой отношение объема жидкости, вышедшей из сосудов, к объему жидкости, остающейся в сосудах [9].
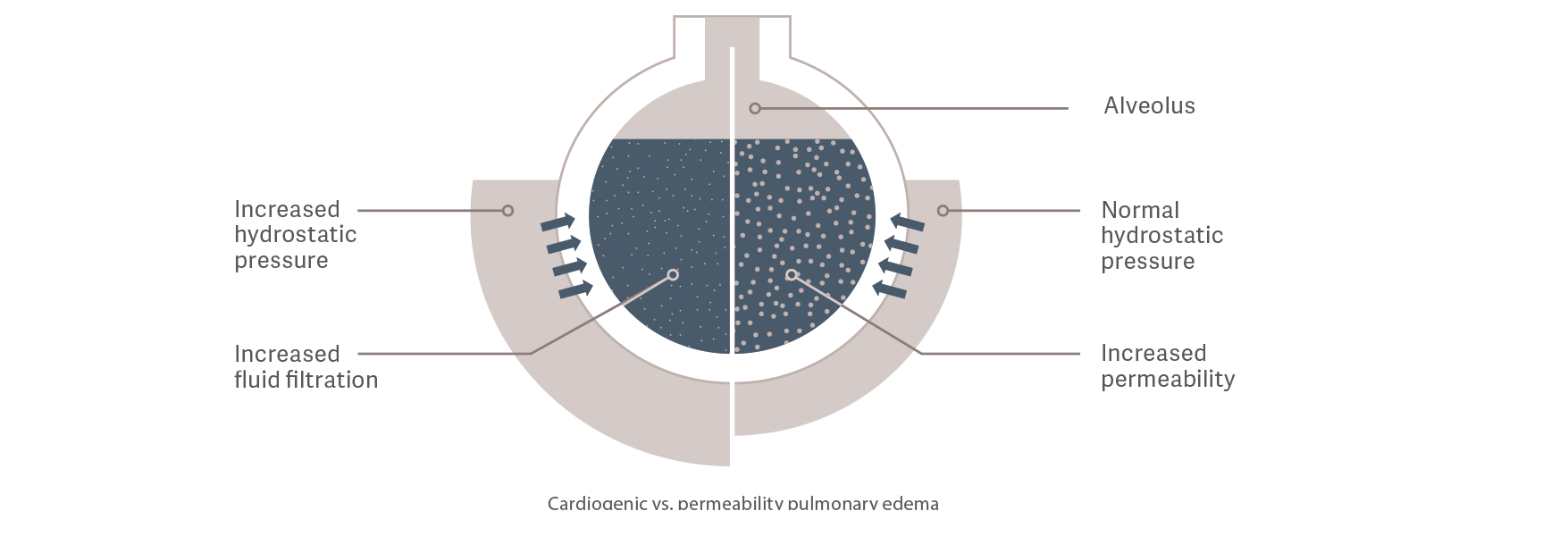
Кардиогенный отек легких
Гидростатическое давление повышается в результате перегрузки внутрисосудистой жидкостью.
Это приводит к выходу жидкостей во внесосудистое пространство.
Отек легких, обусловленный проницаемостью
Проницаемость сосудов повышается в результате воспалительной реакции, вызванной, например, сепсисом. Это приводит к увеличению выхода жидкостей, электролитов
и белков из внутрисосудистого во внесосудистое пространство даже
при нормальном или низком статусе внутрисосудистой жидкости и гидростатическом давлении.
Использование ELWI и PVPI дает клиническое преимущество
Необходимость выявлять и количественно оценивать отек легких при сложных синдромах, таких как ОРДС, может влиять на исход лечения. Нарастание отека легких нарушает газообмен в дыхательных путях, что приводит к дыхательной недостаточности. Параметры ELWI и PVPI можно использовать для чувствительной количественной оценки отека легких у постели больного. Они также позволяют оценить тяжесть ОРДС [2].
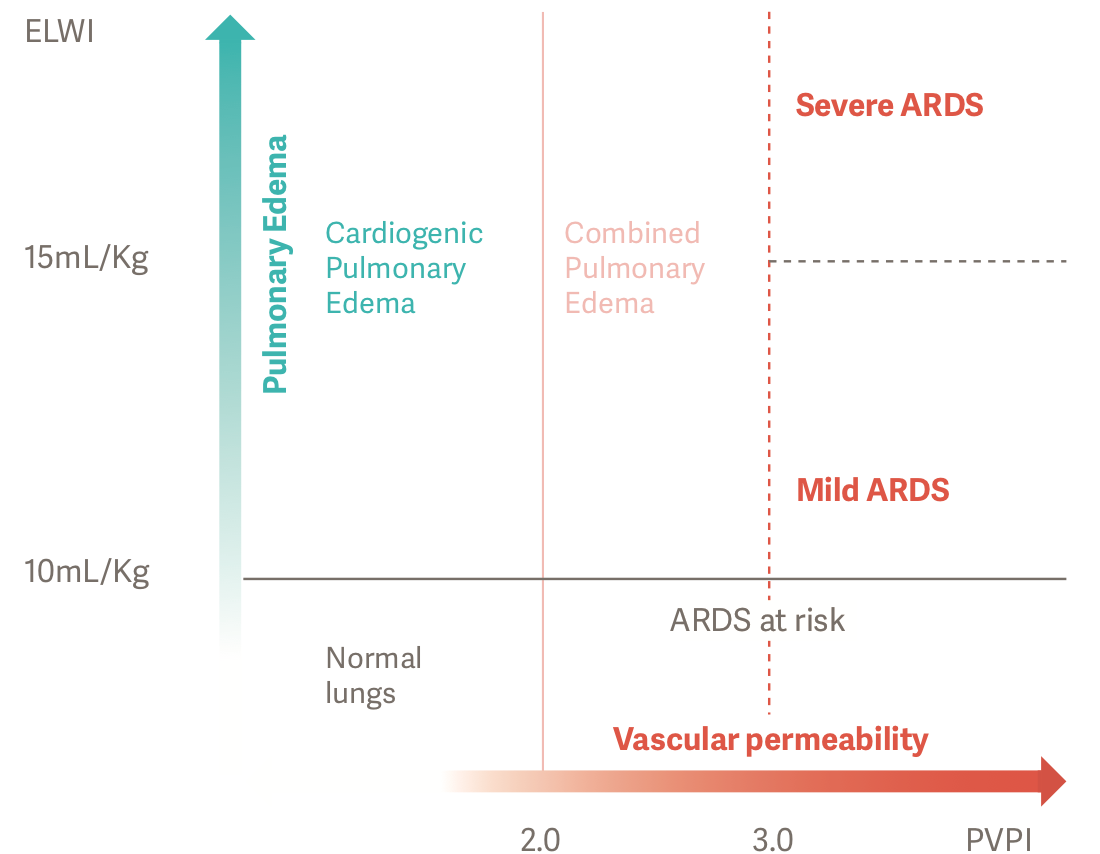
Точную и объективную диагностику у пациентов с ОРДС можно выполнить с использованием ELWI и PVPI. PVPI более 3 при ELWI более 10 мл/кг отражает отек легких, обусловленный повышенной проницаемостью, или ОРДС [2].
Ведение пациентов с ОРДС с использованием PiCCO позволяет улучшать исход лечения
В контексте ОРДС исследования демонстрируют, что ведение пациентов на основе протоколов, включающих измерения ELWI, безопасно, приводит к снижению совокупного жидкостного баланса, снижает смертность в отделениях интенсивной терапии (ОИТ) и сокращает продолжительность искусственной вентиляции легких, а также затраты на пребывание и лечение в БИТ [10].
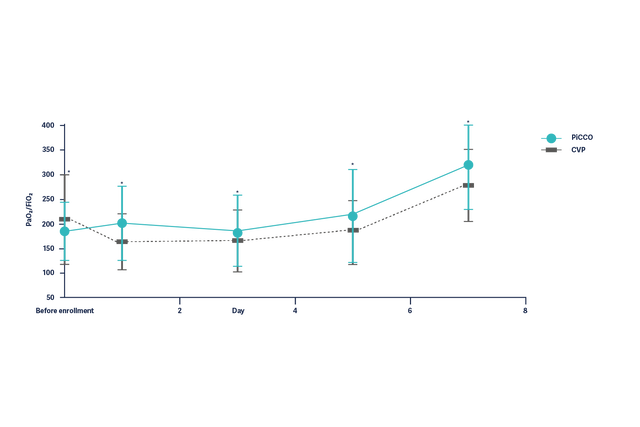
Улучшение оксигенации (PaO2/FiO2) у пациентов с ОРДС в течение 7 дней значительно лучше у пациентов с гемодинамическим контролем на основании параметров PiCCO.