Waarom geavanceerde hemodynamische monitoring?
Het leven van ernstig zieke patiënten met hemodynamische instabiliteit hangt af van de juiste beslissing over de volgende therapeutische stap. Geavanceerde hemodynamische monitoring helpt bij het bepalen van een gerichte en patiëntspecifieke behandeling.
De monitoring van fysiologische parameters van de cardiovasculaire functie is een cruciale factor voor de gerichte behandeling van ernstig zieke patiënten.
Grenzen van basismonitoring
Bij hemodynamische instabiliteit als gevolg van orgaanfalen of een grote operatie bereikt de basismonitoring zijn grenzen. In dergelijke gevallen kan de status van de patiënt in zeer korte tijd snel veranderen. Voor een gedifferentieerde beoordeling van de circulatietoestand zijn de standaardparameters ECG, bloeddrukmeting en pulsoximetrie niet langer voldoende om het hartminuutvolume (CO) en het zuurstoftransport betrouwbaar te beoordelen voor een gerichte, patiëntspecifieke therapie.
Meer gedifferentieerde beoordeling door geavanceerde hemodynamische monitoring
De geavanceerde hemodynamische monitoring biedt aanvullende en veel nauwkeurigere informatie over het cardiovasculaire systeem, zoals bloedstroom, volumestatus, vasculaire tonus en hartfuncties. Door de vorm en de oppervlakte onder de arteriële drukcurve (pulsecontouranalyse), de structurele en mechanische eigenschappen van het vasculaire systeem en de fysische eigenschappen van het bloed continu te bewaken en te analyseren, kan op elk moment een gedifferentieerde beoordeling van de circulatietoestand worden uitgevoerd en een doelgerichte therapie worden gestart.
Bovendien maakt de extravasculaire longwaterindex (ELWI) een bed-side evaluatie van longoedeem mogelijk, zodat in een vroeg stadium therapeutisch kan worden ingegrepen[1][2][3].
Prof. dr. Bernd Christopher Saugel van UKE Hamburg legt uit: “Terwijl de basale hemodynamische monitoring met registratie van hartslag, bloeddruk en andere drukparameters in wezen de functie van veiligheidsbewaking vervult, dient de geavanceerde hemodynamische monitoring om verstoringen van de homeostase aan het licht te brengen nog vóór de vitale functies zijn aangetast." Een gerichte therapiesturing en dus hemodynamisch management, is alleen mogelijk op basis van deze uitgebreide parameters en speciale bewakingstechnologieën[4].
De geavanceerde hemodynamische monitoring maakt antwoorden op de volgende vragen mogelijk:
- Wat is de huidige cardiovasculaire situatie?
- Wat is de cardiale preload en afterload?
- Leidt een toename van de preload tot een hoger hartminuutvolume (reageert de patiënt op vochttoediening)?
- Moet er volume of catecholamines worden toegediend?
- Is er een risico op volumeoverbelasting?
- Ontwikkelt de patiënt longoedeem?
Door het gebruik van geavanceerde hemodynamische monitoring zijn artsen te allen tijde op de hoogte van veranderingen in de toestand van de patiënt. Hierdoor kan de behandeling direct en gericht worden aangepast en kan een patiëntspecifieke behandeling worden uitgevoerd met optimaal gebruik van volume, inotropica en vasoactieve stoffen. Onderzoek heeft aangetoond dat hemodynamische optimalisatie in de context van vroege doelgerichte therapie (Early Goal-Directed Therapy, EGDT) complicaties en morbiditeit vermindert, de verblijfsduur verkort en kosten bespaart[5][6][7].
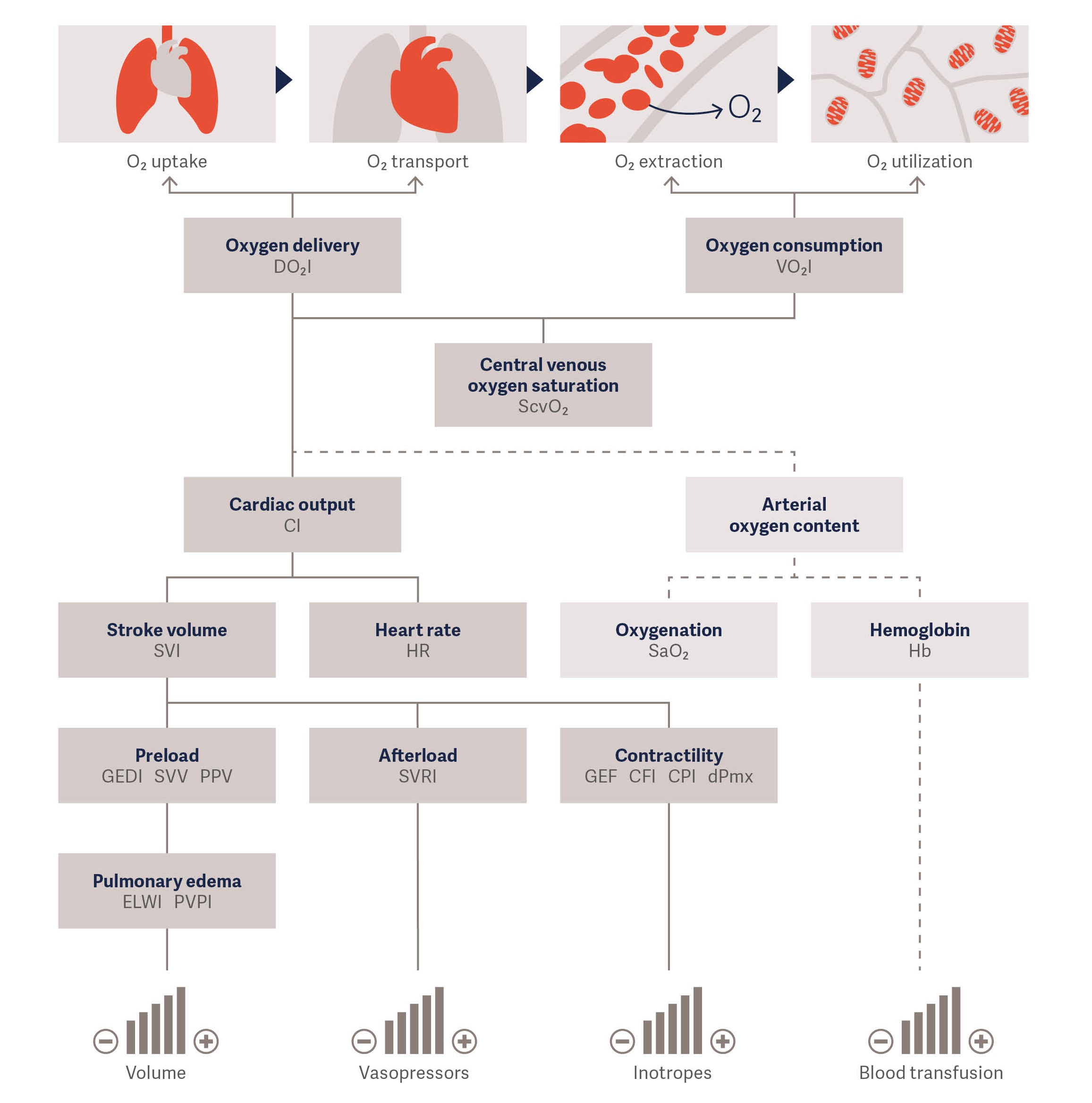
Afbeelding: hemodynamische parameters en hun relaties
Typische indicaties voor het gebruik van geavanceerde hemodynamische monitoring zijn zowel in de intensive care-geneeskunde als in de anesthesie:
- Septische shock
- Acute respiratory distress syndrome (ARDS)
- Cardiogene shock
- Ernstige brandwonden
- Polytrauma
- Pancreatitis
- Chirurgische ingrepen met een hoog risico
- Gerichte vloeistoftherapie
Mark van Iperen van Ziekenhuis Gelderse Vallei in Ede, Nederland: “Wij gebruiken geavanceerde hemodynamische monitoring bij bijna alle patiënten, vooral bij ernstig zieke of hartpatiënten. Monitoring van fysiologische parameters is essentieel voor gerichte behandeling van IC-patiënten.”
De principes van transpulmonale thermodilutie en arteriële pulse-contouranalyse maken de berekening van geavanceerde hemodynamische parameters mogelijk en zijn al meer dan 20 jaar klinisch getest en vastgesteld[8],[9].
