Syndrome de détresse respiratoire aigüe (SDRA)
Le défi de l’identification et du traitement du SDRA

Le défi
Le SDRA est un syndrome qui semble sous-identifié, traité tardivement et associé à un taux de mortalité élevé. L’évolution du SDRA est progressive avec une fenêtre de traitement précoce qui peut être exploitée.[1]
Le SDRA est un type de lésion pulmonaire aiguë diffuse et inflammatoire, entraînant une perméabilité vasculaire pulmonaire accrue, une augmentation du poids des poumons et une perte de tissu pulmonaire aéré » (La définition de Berlin du SDRA). Elle est associée à une mortalité élevée et peut être causée par plusieurs étiologies.
Les soins prodigués aux patients atteints de SDRA sont complexes et associés à de longues hospitalisations ; ils nécessitent également d’importantes ressources en soins de santé.[2] Il semble que les approches recommandées pour la ventilation mécanique et l’application de certaines mesures d’appoint soient peu utilisées dans le cadre du traitement du SDRA. Ces informations indiquent qu’il existe donc un potentiel d’amélioration de la prise en charge des patients atteints de SDRA.[1]
Signes et symptômes cliniques du SDRA
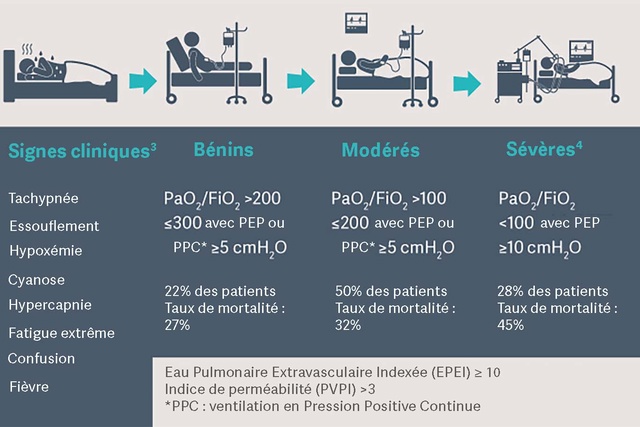
Les recommandations actuelles
American Thoracic Society / European Society of Intensive Care Medicine / Society of Critical Care Medicine
Directive de pratique clinique :
Ventilation mécanique chez les patients adultes atteints du syndrome de détresse respiratoire aiguë[5],[6]
Traitement |
Recommandation |
Force de la recommandation |
|
Ventilation mécanique à l’aide de faibles volumes courants et pressions inspiratoires |
Recommander que les patients adultes atteints de SDRA bénéficient d’une ventilation mécanique avec des volumes courants limités à 4-8 ml/kg de PP et des pressions de plateau inspiratoires < 30 cm H2O |
Forte recommandation avec confiance modérée sur l’effet estimé |
|
Décubitus ventral |
Recommander que les patients adultes atteints de SDRA sévère restent en décubitus ventral pendant plus de 12 heures par jour |
Forte recommandation avec une confiance modérée à élevée sur l’effet estimé |
|
PEP élevée versus PEP basse |
Suggérer que les patients adultes atteints d’un SDRA modéré ou sévère reçoivent des niveaux de PEP plutôt élevés que bas |
Recommandation sous conditions avec une confiance modérée sur l’effet estimé |
|
Manœuvres de recrutement (MR) |
Suggérer que les patients adultes atteints de SDRA reçoivent des MR |
Recommandation sous conditions avec une confiance modérée sur l’effet estimé |
|
Oxygénation par membrane extracorporelle (ECMO) |
Des éléments probants supplémentaires sont nécessaires pour effectuer une recommandation définitive pour ou contre l’usage de l’ECMO chez les patients atteints de SDRA sévère |
Recommander des recherches continues évaluant les résultats cliniques des patients atteints de SDRA sévère recevant une ECMO |
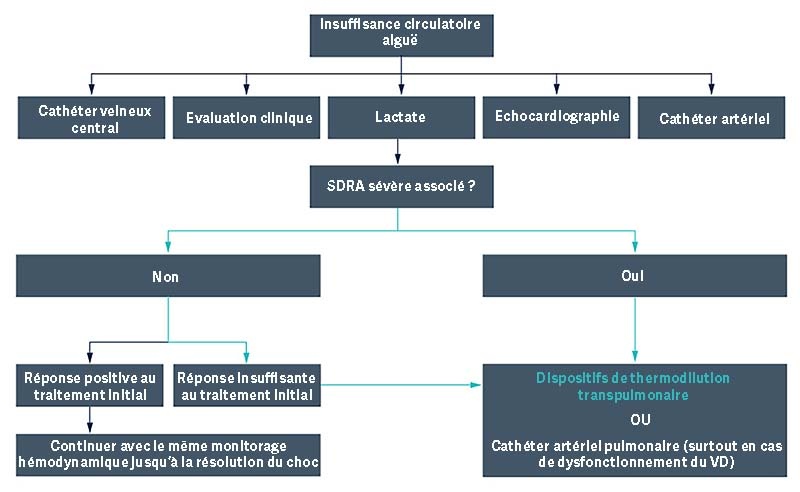
L’importance de connaître l’état du remplissage
Chaque jour en réanimation, les cliniciens doivent faire face à ce dilemme thérapeutique pour le patient atteint d’une insuffisance circulatoire et d’atteinte pulmonaire : dois-je opter pour un remplissage ?
En cas de SDRA sévère associé à un choc, il a été suggéré d’envisager d’utiliser des dispositifs de surveillance avancés à une phase précoce pour aider à définir une approche thérapeutique logique.
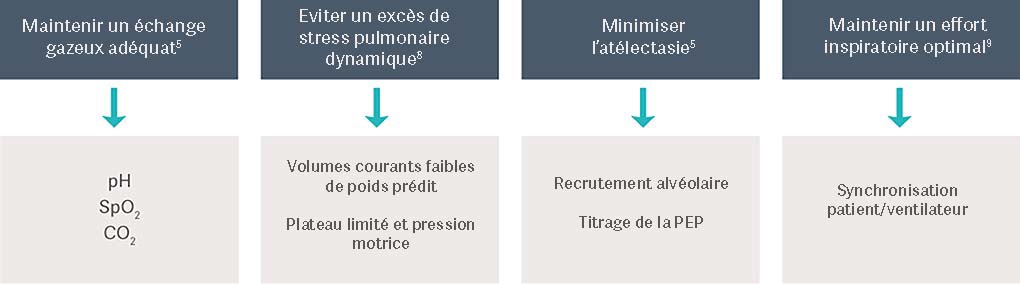
L’objectif de la ventilation
« L’objectif de la ventilation mécanique chez les patients atteints de SDRA est de maintenir les échanges gazeux tout en évitant les complications telles que des lésions pulmonaires induites par le ventilateur (LPIV), une pneumonie acquise sous ventilation (PAV) ou une dysfonction du diaphragme induite par la ventilation (DDIV) »[5]

Diagnostic de l’œdème pulmonaire au chevet du patient
Le SDRA se caractérise par un œdème pulmonaire qui est l’accumulation de fluide dans les interstices du tissu pulmonaire et/ou dans les alvéoles. Cela entraîne des perturbations de l’échange gazeux et peut même provoquer une défaillance pulmonaire. L’importance de l’œdème pulmonaire peut être quantifiée très simplement au chevet du patient par une mesure de l’eau pulmonaire extravasculaire indexée (EPEI). La question importante à se poser est la suivante : quelle est la cause de l’œdème pulmonaire ? L’indice de perméabilité vasculaire pulmonaire (PVPI) permet un diagnostic différentiel. En cas d’œdème pulmonaire cardiogénique, un bilan liquidien négatif sera visé, tandis qu’il faudra lutter en premier lieu contre la cause de l’inflammation en cas d’œdème pulmonaire de perméabilité.

ECMO pour le traitement du SDRA
L’oxygénation par membrane extra-corporelle (ECMO) pour l’insuffisance respiratoire aigüe a été proposée il y a plus de 40 ans.[10] Par la suite, des améliorations technologiques ont permis d’optimiser la sécurité et la facilité d’utilisation de l’ECMO et de l’utiliser ainsi plus largement dans les cas d’insuffisance respiratoire aigüe.[11]
L’ECMO VV (veino-veineuse) est devenue le traitement de choix pour les patients souffrant d’insuffisance respiratoire réfractaires à une ventilation mécanique optimale et aux traitements médicaux conventionnels.[12]
Oxygénation par membrane extra-corporelle
pour le syndrome de détresse respiratoire aiguë sévère
L’étude EOLIA
L’efficacité de l’oxygénation par membrane extra-corporelle (ECMO) veino-veineuse chez les patients atteints du syndrome de détresse respiratoire aiguë sévère (SDRA) reste controversée. L’étude [13] EOLIA a été conçue pour déterminer l’effet de l’initiation précoce de l’ECMO chez les patients atteints des formes les plus sévères de SDRA.[1]
ECMO précoce
35 % de mortalité
(44/124)
249 patients
124 ont bénéficié d’une ECMO VV et
125 d’un traitement conventionnel
Ventilation conventionnelle*
46% de mortalité
(57/125)