Herausforderung:
Optimierung der Volumentherapie bei ARDS-Patientinnen und -Patienten
Das Leben einer kritisch kranken Patientin oder eines kritisch kranken Patienten hängt von der richtigen Entscheidung über den nächsten therapeutischen Schritt ab. Bei einem ARDS gilt dies um so mehr, da die geschädigte Lunge eine erhöhte vaskuläre Permeabilität aufweist, die zu einem Lungenödem führt. Die Notwendigkeit sich frühzeitig ein vollständiges Bildes des hämodynamischen Zustands der Patientin/des Patienten zu verschaffen, ist für eine adäquate Therapie von entscheidender Bedeutung. Der Zeitpunkt des Therapiebeginns hat Einfluss auf das Ergebnis.
Können wir ein Lungenödem quantifizieren?
Zur Quantifizierung eines Lungenödems unter Verwendung des extravaskulären Lungenwasserindex (ELWI) und des pulmonalvaskulären Permeabilitätsindex (PVPI) hat sich die Verwendung der transpulmonalen Thermodilution (TPTD) etabliert . Der PVPI ermöglicht die Differenzialdiagnose des Ursprungs eines Lungenödems: kardiogen oder permeabilitätsbedingt. ELWI und PVPI können als Kriterien für das Risiko einer Volumengabe verwendet werden. [2]
Als extravaskuläres Lungenwasser bezeichnet man die intrazelluläre, interstitielle und intraalveoläre Flüssigkeit in der Lunge. Der pulmonalvaskuläre Permeabilitätsindex (PVPI) ist ein indirektes Spiegelbild der Integrität der Blut-Luft-Schranke.
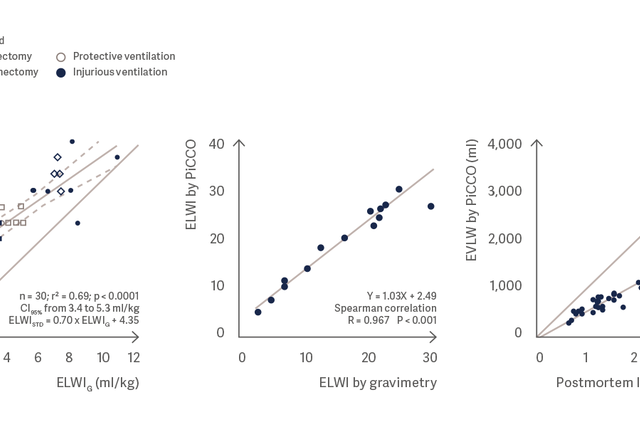
Die Messung des Lungenwassers mittels PiCCO korreliert sehr gut mit der gravimetrischen Bestimmung des Lungenwassers sowie dem postmortalen Lungengewicht. [3], [4], [5]
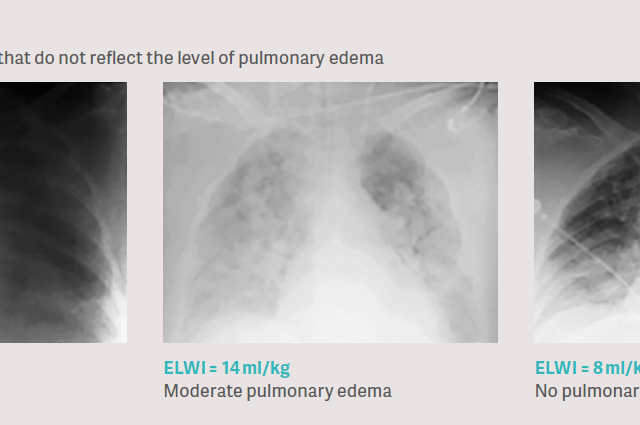
Klinische Probleme: Röntgen-Aufnahmen des Brustkorbs sind bei der Beurteilung des Schweregrads eines Lungenödems nicht ausreichend zuverlässig.
Der übliche klinische Ansatz zur Untersuchung eines Lungenödems ist die Beurteilung einer Thorax-Röntgenaufnahme. Diese Beurteilung ist u. U. schwierig, da die Röntgenaufnahme des Brustkorbs eine Dichtemessung darstellt, die von Knochen, Muskeln, Gewebeschichten/-ödem, Blut, Blutgefäßen, Luft, Pleuraerguss und möglicherweise auch einem Lungenödem beeinflusst wird. In klinischen Studien wurde gezeigt, dass die röntgenologische Abschätzung von Lungenödemen im Vergleich zur direkten Quantifizierung durch transpulmonale Thermodilution sehr ungenau ist. [6], [7], [8].
Kardiogenes oder Permeabilitäts-Lungenödem?
Der PVPI reflektiert indirekt die Integrität der
Blut-Luft-Schranke. Der Wert wird aus dem Verhältnis zwischen Lungenwasserindex (ELWI) und pulmonalem Blutvolumen (PBV) berechnet, d. h. aus dem Verhältnis zwischen extravaskulären und intravaskulären Flüssigkeitsvolumen [9]
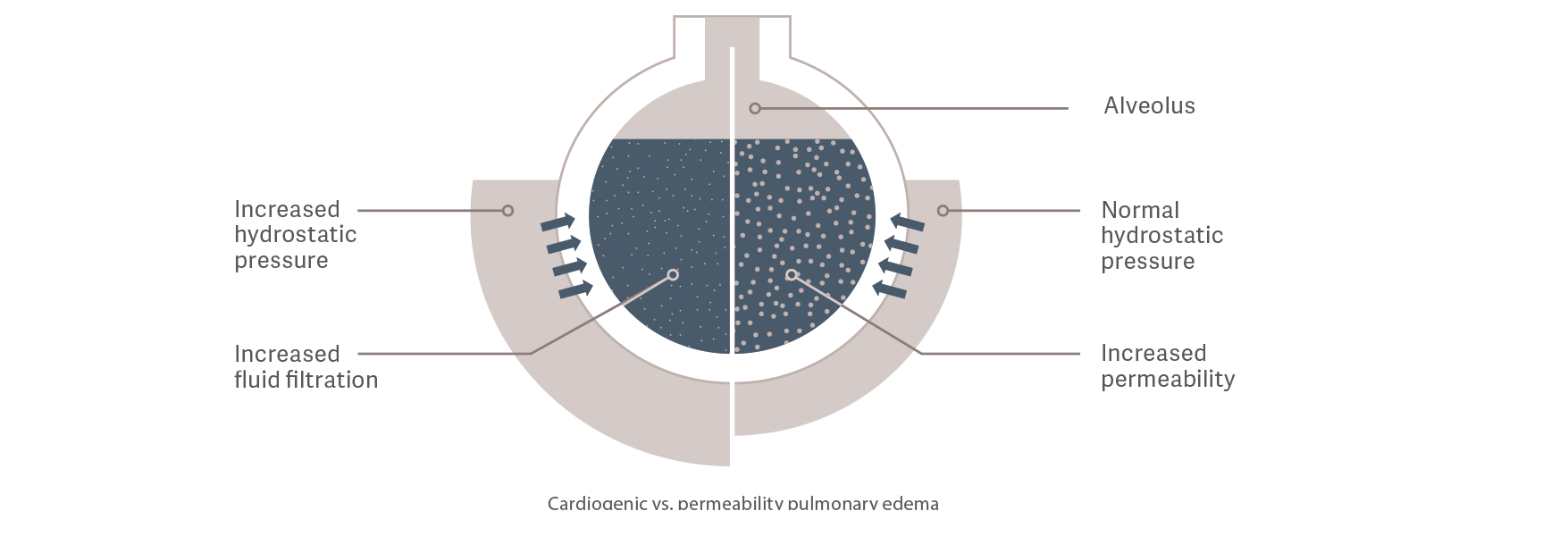
Kardiogenes Lungenödem
Der hydrostatische Druck steigt infolge einer zu großen Menge intravaskulärer Flüssigkeit.
Hierdurch kommt es zum Austritt von Flüssigkeit in den extravaskulären Raum.
Permeabilitäts-Lungenödem
Die vaskuläre Permeabilität nimmt in Folge einer Entzündungsreaktion (z. B. durch Sepsis) zu. Dies führt, trotz normalem bis niedrigen intravaskulären Flüssigkeitsstatus und hydrostatischen Druck, zu einem gesteigerten Austritt von Elektrolyten
und Proteinen sowie in Folge dessen von Flüssigkeit, aus dem intravaskulären in den extravaskulären Raum.
Die Interaktion von ELWI und PVPI ist von klinischem Nutzen
Die Erkennung und Quantifizierung eines Lungenödems bei komplexen Syndromen wie dem ARDS, kann das Behandlungsergebnis positiv beeinflussen. Ein pulmonales Ödem beeinträchtigt den Gasaustausch und führt in Folge dessen zur Hypoxämie. Mit den Parametern ELWI und PVPI kann ein Lungenödem bettseitig sensibel quantifiziert werden. Damit wird die Einschätzung des ARDS-Schweregrades möglich. [2]
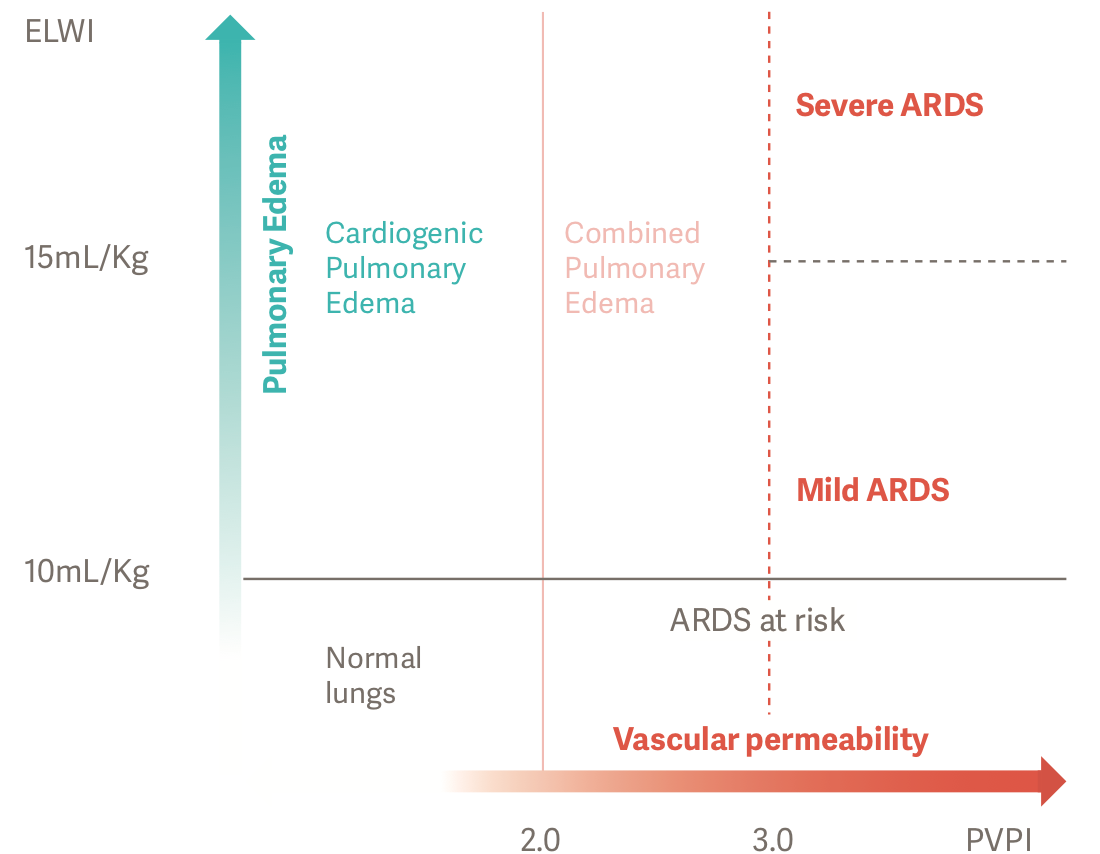
Unter Zuhilfenahme von ELWI und PVPI können präzise und objektive Diagnosen bei ARDS-Patientinnen und -Patienten gestellt werden. Ein PVPI > 3 bei einem ELWI > 10 ml/kg lässt auf ein Lungenödem mit erhöhter Permeabilität oder auf ARDS schließen.[2]
Ein ARDS-Management basierend auf PiCCO Parameter führt zu besseren Ergebnissen
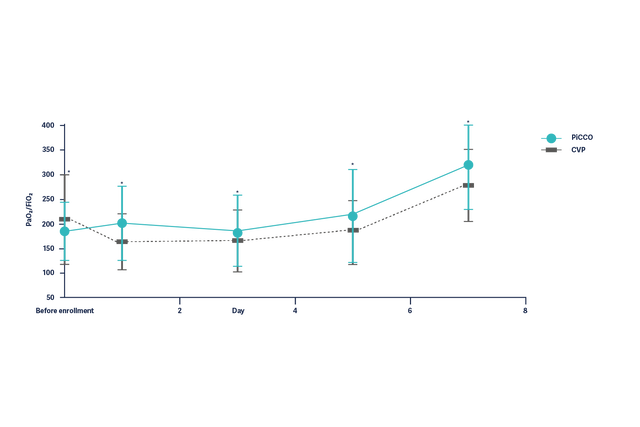
Im Zusammenhang mit ARDS deuten Studien darauf hin, dass das ein Protokoll- basiertes Management, einschließlich ELWI-Messungen, sicher ist, zu einer geringeren kumulativen Flüssigkeitsbilanz führt, die Mortalität auf der Intensivstation senkt, die Dauer der maschinellen Beatmung sowie die Verweildauer auf der Intensivstation und die Behandlungskosten reduziert. [10]
Die Verbesserung der Oxygenierung (PaO2/FiO2) bei ARDS-Patientinnen und -Patienten über 7 Tage ist bei Patientinnen und Patienten mit hämodynamischem Management basierend auf PiCCO-Parametern signifikant höher.