客户通知函
迈柯唯(上海)医疗设备公司报告,生产企业调查发现制造过程中GDS组件压接不充分,导致人造血管的Slider GDS移植体放置系统的转杆和锚之间存在间隙。生产企业目前尚未收到因上述问题导致用户伤害的不良事件。
本着对客户负责的态度,确保设备使用安全、有效,经生产企业评估后决定对其生产的人造血管 Flixene vascular grafts(注册证号:国械注进20163130143)主动召回。召回级别为二级。

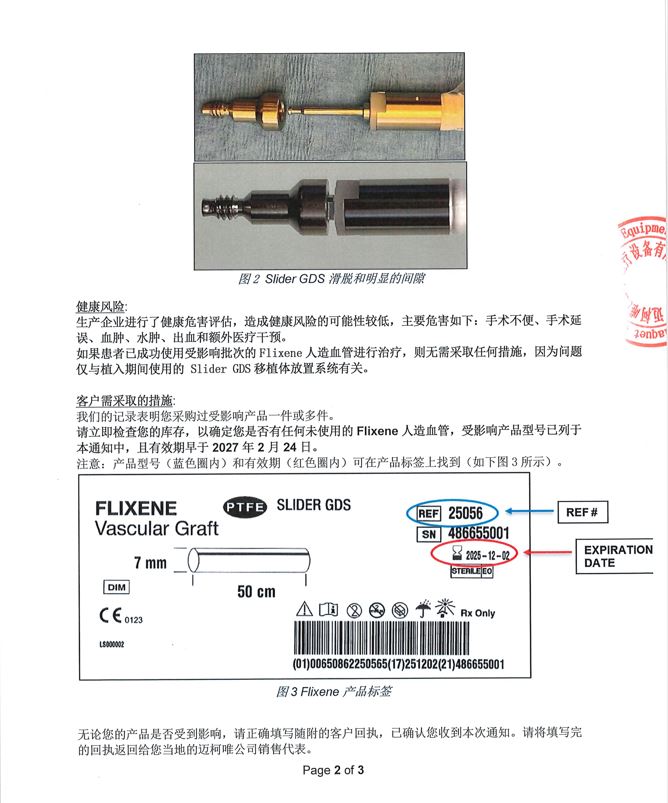

迈柯唯(上海)医疗设备公司报告,生产企业调查发现制造过程中GDS组件压接不充分,导致人造血管的Slider GDS移植体放置系统的转杆和锚之间存在间隙。生产企业目前尚未收到因上述问题导致用户伤害的不良事件。
本着对客户负责的态度,确保设备使用安全、有效,经生产企业评估后决定对其生产的人造血管 Flixene vascular grafts(注册证号:国械注进20163130143)主动召回。召回级别为二级。



您现在正离开Getinge.com。您可能会访问非Getinge团队管理的内容,在这种情况下,Getinge对这些内容不负责任。